Foram encontradas 1.668 questões.
Nos últimos anos, a lactose vem sendo classificada como um dos grandes vilões da boa alimentação. Milhares de pessoas aboliram esse nutriente do cardápio e o mercado de produtos sem lactose vem crescendo cada vez mais. A intolerância à lactose é um distúrbio metabólico bastante comum em adultos humanos, causada por baixos níveis no organismo da enzima lactase, responsável por clivar a lactose em galactose e glicose. Nessas pessoas, boa parte da lactose ingerida atravessa o trato digestivo e chega ao cólon, em que a fermentação bacteriana leva à formação de grandes quantidades de gases e compostos orgânicos irritantes, que causam desconforto e dores abdominais.
Com base no texto acima e na estrutura da lactose, mostrada abaixo, leia com atenção as afirmações a seguir sobre a bioquímica de carboidratos e marque (V) para as verdadeiras e (F) para as falsas.
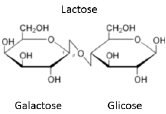
Fonte: Site Fisiculturismo Brasil
( ) A lactose pode ser classificada como um dissacarídeo, uma vez que é composta por dois monossacarídeos unidos por uma ligação peptídica.
( ) A galactose e a glicose são exemplos de furanoses e, no caso da lactose, estão unidas por uma ligação (1 4).
( ) A lactose é classificada como um açúcar redutor, pois a galactose possui um carbono anomérico livre.
( ) A representação utilizada para a estrutura da lactose, mostrada acima, é chamada de projeção de Newmann.
( ) Na estrutura acima, observa-se que a glicose está representada na forma de anômero β.
Assinale a alternativa que contém a sequência CORRETA, de cima para baixo.
Provas
O 2,4,5-T (ácido 2,4,5-triclorofenoxiacético) é um herbicida que foi muito utilizado pelo exército dos Estados Unidos na Guerra do Vietnã, como um dos componentes do agente laranja, um poderoso desfolhante. O 2,4,5-T é preparado pela sequência de reações mostrada abaixo.
Em relação ao texto e à equação apresentada, todas as alternativas abaixo estão corretas, EXCETO UMA, assinale-a.
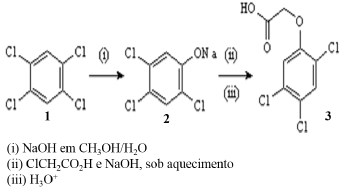
Fonte: Site da Escola de Química da Universidade de Bristol
Provas
A estrutura abaixo representa a cisteína.
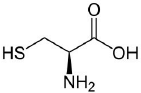
Assinale a alternativa que indica CORRETAMENTE os grupos funcionais presentes na molécula de cisteína.
Provas
O carbonato de sódio é um sal branco e translúcido, usado na produção de vidro. É possível obter o carbonato de sódio por meio da reação:
!$ 2 Na C \ell_{(aq)} + Ca CO_{3(aq)} \rightarrow Na_2 CO_{3(aq)} + CaC\ell_{2(aq)} !$
Qual a massa de carbonato de sódio obtida pela reação de 500 g de carbonato de cálcio, 70% puro, sabendo que o rendimento da reação é de 90%?
Assinale a alternativa que indica CORRETAMENTE a massa de carbonato de sódio obtida.
Provas
As pilhas comuns ou pilhas secas são também conhecidas como pilhas de Leclanché, em homenagem ao químico George Leclanché que desenvolveu esse tipo de pilha no ano de1866.
Essa pilha é formada por um ânodo de zinco metálico, separado das demais espécies químicas por um papel poroso. O eletrodo central é o cátodo que consiste de grafite coberto por uma camada de dióxido de Manganês, carvão em pó e uma pasta contendo cloreto de amônio ecloreto de zinco.
No polo negativo:
!$ Zn_{(s)} \rightarrow Zn_{(aq)}^{2+} + 2\,e^- !$
No poló positivo:
!$ 2 MnO_{2(aq)} + 2NH_{4(aq)}^+ 2e^- \rightarrow Mn_2O_{3(s)}+ H_2 O_{ (\ell)} !$
Sabendo que a pilha de Leclanché fornece uma força eletromotriz de 1,50 V e que o potencial de oxidação do zinco é igual a +0,76 V, assinale a alternativa que corresponde CORRETAMENTE ao potencial de redução-padrão do cátodo.
Provas
Sobre uma bancada de laboratório foi encontrado um frasco de solução com a etiqueta borrada, a única informação possível de se identificar era de que se tratava de uma solução de H2SO4(aq). Para identificar a concentração dessa solução, separou-se uma alíquota de 10 mL de H2SO4(aq) , que foi titulado com uma solução NaOH(aq) 1mol/L, sendo gastos 15 mL dessa base. Assinale a alternativa que informa CORRETAMENTE a concentração da solução de H2SO4(aq) contida no frasco.
Provas
Dos compostos abaixo, verifique os que apresentam atividade óptica.
I. 3-metilpentan-2-ona
II. propan-2-ol
III. butan-2-ol
IV. 2-metilbutan-2-ol
V. 3-metilpent-1-eno
Assinale a alternativa que apresenta somente os itens CORRETOS.
Provas
Sobre o modelo atômico de Bohr, assinale a alternativa INCORRETA.
Provas
Em processos isotérmicos, pode-se determinar a variação da Energia Livre de Gibbs apenas pela variação da entalpia e da entropia do sistema na temperatura estudada.
Sendo assim, e com base na tabela abaixo, avalie as afirmativas abaixo e marque V para as verdadeiras e F para as falsas, quanto à reação de formação da água.
| H2 (g) | O2 (g) |
H2O (l) |
|
|
!$ \triangle_f !$H, kJ/mol S, J/mol·K |
0 131 |
0 205 |
-286 70 |
( ) A reação será espontânea em temperaturas inferiores a 1400ºC.
( ) Não será possível realizar essa reação espontaneamente em temperaturas superiores a 100º C.
( ) Há um aumento na entropia do sistema, o que torna essa reação espontânea.
( ) Essa reação não é espontânea em qualquer temperatura.
( ) A temperatura ambiente essa reação é espontânea.
Assinale a alternativa que apresenta a sequência CORRETA de cima para baixo.
Provas
Polímeros são macromoléculas que possuem unidades químicas repetidas regularmente ao longo da cadeia, denominadas meros.
Avalie as afirmações abaixo que descrevem algumas características dos polímeros.
I. Os polímeros de adição são macromoléculas formadas a partir de monômeros com a eliminação de pequenas moléculas.
II. Os polímeros de adição podem ser formados a partir de monômeros vinílicos que têm dupla ligação.
III. As resinas são sólidos ou líquidos muito viscosos à temperatura ambiente que amolecem gradualmente com o aumento da temperatura.
IV. Os termorrígidos são polímeros que apresentam as características de fusibilidade e solubilidade aumentados, em condições de baixa pressão.
V. Polímero é um composto químico de peso molecular elevado e variado.
Assinale a alternativa que apresenta somente as afirmações CORRETAS.
Provas
Caderno Container