Foram encontradas 1.668 questões.
Verificando-se que, em uma determinada temperatura, a solução saturada de um hidróxido de um metal alcalino- terroso apresenta pH = 9, assinale a alternativa que descreve a solubilidade CORRETA desse composto.
Provas
O elétron mais energético de elemento químico possui os seguintes números quânticos: n = 3; l = 1; m = -1; s = + ½. Acerca desse elemento, assinale a alternativa CORRETA.
Provas
Segundo Brönsted e Lowry, ácidos são substâncias ou partículas capazes de ceder cátions H+ (prótons) e as bases são substâncias ou partículas capazes de aceitar cátions H+, portanto reações ácido-base são reações químicas que envolvem a transferência de prótons. Considerando os ácidos e as bases em meio aquoso, assinale a alternativa CORRETA.
Provas
Nos últimos anos, com o aumento da oferta de diferentes variedades de produtos alimentícios, cada vez mais é necessário se ter o conhecimento sobre a composição dos alimentos. Nesse contexto, a leitura de rótulos permite saber porque e quando não devemos comprar um certo alimento, para que não sejam ingeridas substâncias que prejudiciais à saúde. Nesse sentido, a Química Analítica desempenha papel fundamental e, em muitos casos, métodos simples são usados na determinação da composição dos alimentos. Por exemplo, a determinação do teor de ácido acético no vinagre pode ser feita seguindo o procedimento a seguir: colocar uma alíquota de 10,0 mL de vinagre em um balão volumétrico de 100,0 mL e completar com água. Em seguida titular 10,0 mL da solução diluída, utilizando uma solução padrão de NaOH 0,040 mol L-1. Considerando que, nesse experimento, foram consumidos 25 mL da solução de NaOH, e que o ácido acético é o único componente ácido do vinagre, conclui-se que a massa em gramas de ácido acético em 1 L do vinagre é de .
(Dados – massas molares: H = 1 g/mol, C = 12 g/mol, O = 16 g/mol, Na = 23 g/mol)
Assinale a alternativa que CORRETAMENTE preenche a lacuna do texto acima.
Provas
A química, ciência responsável por grande parte dos benefícios e da qualidade de vida do homem, é encarada como responsável por vários problemas ambientais. De fato, o uso inadequado de algumas substâncias e o descarte inadequado de resíduos têm gerado impactos negativos ao meio ambiente. Assim, a formação de futuros profissionais em química deve conter itens que enfatizem a problemática ambiental a fim de que estejam preparados para lidar com propriedade sobre essa situação tão inquietante. A educação ambiental (EA) entra nesse cenário, exigindo um redimensionamento das práticas pedagógicas para um saber ambiental articulado com a prática social. Nos PCN, a EA é um dos temas transversais, e deve ser trabalhada enfatizando-se aspectos sociais, econômicos, políticos e ecológicos.
De acordo com os PCN, todas as alternativas abaixo apresentam princípios da EA, definidos na Conferência Intergovernamental de Educação Ambiental, EXCETO UMA, assinale-a.
Provas
Em um ecossistema, plantas e animais necessitam de suprimento constante de energia e nutrientes para sobreviverem. Os nutrientes são frequentemente reciclados e reutilizados. Quando seres vivos morrem, seus tecidos se decompõem e compostos químicos vitais retornam ao solo, à água e à atmosfera. Mais de 95% da massa dos tecidos dos seres vivos é composta pelos seguintes elementos: carbono, hidrogênio, oxigênio, nitrogênio, enxofre e fósforo, os quais são utilizados na biossíntese de carboidratos, proteínas e lipídeos. As plantas obtêm os elementos essenciais do solo e da atmosfera, já os animais os obtém principalmente pela alimentação.
Na figura abaixo é mostrado o ciclo do carbono.
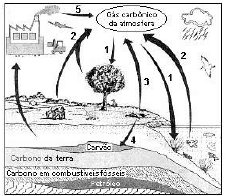
Fonte: Google Sites
Assinale a alternativa que apresenta a principal fonte de carbono do planeta Terra.
Provas
Diversos compostos exibem colorações que dependem do pH da solução na qual estão dissolvidos. Muitos desses compostos são utilizados para indicar a acidez ou alcalinidade de soluções aquosas e são chamados de indicadores ácido/base. Um indicador ácido/base é uma base ou ácido orgânico fraco cuja coloração é diferente da coloração de seu ácido ou base conjugados. Abaixo são mostradas duas formas (dissociada e não-dissociada) do indicador azul de bromotimol (pKa = 7,10) e suas respectivas colorações. Com base no texto acima e nas estruturas abaixo, marque (V) para as alternativas verdadeiras e (F) para as falsas.
( ) Com base no valor do pKa do azul de bromotimol, é possível afirmar que sua faixa de transição de pH é de 1,2 a 2,8.
( ) O azul de bromotimol é classificado como um indicador do tipo ácido (HIn) e o seu comportamento em meio aquoso é dado pela equação HIn + H2O In- + H3O+.
( ) Diversos fatores influenciam a faixa de transição de um indicador, como a temperatura e a força iônica do meio.
( ) O azul de bromotimol adquire coloração amarela em pH = 10.
( ) Ambas as formas do azul de bromotimol apresentadas possuem a função orgânica álcool em suas estruturas.
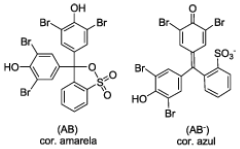
Site da revista Química Nova
Assinale a alternativa que contém a sequência CORRETA, de cima para baixo.
Provas
A técnica de datação com carbono radioativo é utilizada para datar achados arqueológicos. O carbono existe na natureza majoritariamente como o isótopo 12C e como uma pequena porcentagem de 13C. O bombardeamento do 14N com nêutrons cósmicos na atmosfera leva à formação do isótopo 14C.
!$ ^{14}_7N +\,\,\, ^{1}_0n\,\,\,^{14}_6C\,\,\,^{1}_1H !$
Esse isótopo é levemente radioativo e tem meia vida de 5668 anos. O isótopo 14C reage com oxigênio do ar, formando 14CO2, o qual é assimilado pelas plantas na fotossíntese e pelos demais seres vivos da cadeia alimentar. A medida da velocidade do decaimento do 14C em uma amostra de couro, madeira, tecido, etc permite calcular a quanto tempo a planta ou o animal morreram.
Qual termo descreve CORRETAMENTE a relação entre os átomos de !$ ^{14}_7N !$ e !$ ^{14}_6C !$
Assinale a alternativa que responde CORRETAMENTE à questão acima.
Provas
A química orgânica do século XX contribuiu significativamente para a melhora na qualidade de vida das pessoas, fornecendo diversos produtos, como medicamentos, plásticos, insumos agrícolas e corantes. Porém, os processos para obtenção desses itens geram resíduos que precisam ser tratados e descartados de forma adequada. Nesse contexto, o crescimento da demanda por processos ambientalmente responsáveis fez surgir um movimento chamado química verde, que engloba um conjunto de ações para nortear o desenvolvimento e a implantação de produtos e processos químicos com reduzido impacto ambiental. Existem 12 princípios de química verde, dentre os quais está a economia atômica: “reações químicas devem ser planejadas de forma a maximizar a incorporação de todos os átomos dos reagentes no produto final”. A fabricação do ibuprofeno, um fármaco com atividade anti-inflamatória, antipirética e analgésica, produzido na escala de 3 milhões de quilos por ano, cuja síntese está mostrada abaixo, engloba vários dos princípios da química verde.
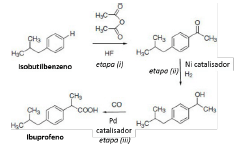
Fonte: Site da Editora Wiley
Dentre as etapas (i), (ii) e (iii), mostradas na síntese acima, aquela(s) que apresenta(m) menor economia atômica está (ão) mostrada(s) em uma das alternativas abaixo. Assinale-a.
Provas
O conhecimento das relações entre estrutura molecular e propriedades físicas permite a previsão dessas propriedades para diferentes compostos, o que pode determinar, por exemplo, a escolha de um solvente para uma certa aplicação. O ponto de ebulição, por exemplo, depende das forças atrativas que existem entre as moléculas de um composto e essas forças, por sua vez, são determinadas pela própria estrutura do composto. Se as forças que mantêm as moléculas unidas no estado líquido forem fortes, muita energia será necessária para separar essas moléculas e o ponto de ebulição da substância será alto.
Associe a coluna da direita com a da esquerda, relacionando corretamente os compostos aos seus respectivos pontos de ebulição.
(1) -162 ºC
(2) -89 ºC
(3) 36 ºC
(4) 140 ºC
(5) 290 ºC
( ) 1,2,3-propanotriol.
( ) metano
( ) etano
( ) ciclopentanol
( ) pentano
Assinale a alternativa que contém a ordem CORRETA de associação, de cima para baixo.
Provas
Caderno Container