Foram encontradas 305 questões.
Por definição, uma solução tampão resiste a variações no pH decorrentes da diluição ou da adição de ácidos ou bases. Os químicos empregam as soluções tampão para manter o pH de soluções sob níveis predeterminados relativamente constantes.
Um estudante misturou 200mL de solução de ácido HX de concentração 0,1mol/L com 300mL de solução do sal de sódio desse ácido (NaX) que tinha concentração de 0,2mol/L. Sabendo que a constante de ionização do ácido HX é 0,000003. Qual o valor do pH da solução formada?
Provas
Uma solução de permanganato de potássio foi colocada em uma cubeta de 2cm de comprimento óptico. Feita a leitura em um equipamento espectrofotômetro UV-Vis, observou-se a absorbância medida de 0,200. Sabendo que o coeficiente de absortividade molar era de 20L.mol-1.cm-1, admite-se que a concentração da solução é de:
Provas
Uma indústria de sanitizantes faz o preparo de álcool líquido 70% INPM (concentração em massa) através da adição de: etanol hidratado 96% (porcentagem em volume) água desnaturante (quantidade desprezível).
Em uma das bateladas de 1000 litros de produto, o analista de controle de qualidade identificou que a concentração alcoólica estava em 70% em volume.
O que o operador deve fazer, desconsiderando as possíveis contrações ou dilatações de volume, para que a indústria entregue um produto com concentração próxima e não inferior a 70% INPM (equivalente à 74,5% em volume)?
Dados de densidade: água= 1,0g/mL; etanol= 0,8g/mL.
Provas
Quimicamente, a cloroquina (CQ) e a hidroxicloroquina (HCQ) pertencem à classe das 4-aminoquinodinas. Elas têm estrutura central aromática comum, com um cloro na posição 7, ligada às respectivas cadeias laterais básicas. A forma molecular da cloroquina é: C18H26CIN3, com massa molar de 319,9 g/mol. Já a hidroxicloroquina tem massa molar de 335,9 g/mol
.
A CQ e a HCQ são administradas como difosfato e sulfato, respectivamente, em suas formas racêmicas.
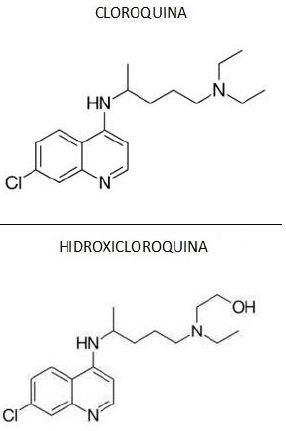
Sobre o medicamento citado acima, marque o que for correto.
Provas
Um mol de uma dada substância é aquecido de 80 °C para 110 °C, sem alterar o seu estado físico. Baseado nos seus conhecimentos de termodinâmica, analise as afirmativas abaixo:
I. A equação !$ \triangle H '= \int_{80}^{110} c_p dT !$ pode ser usada para calcular a variação da entalpia associado ao aquecimento de um mol da substância.
II. Se a substância for um líquido ou sólido, o processo de aquecimento terá praticamente o mesmo gasto energético a volume constante e a pressão constante.
III. Se a substância for um gás ideal, o processo de aquecimento a pressão constante gastará mais energia que o processo de aquecimento a volume constante.
Assinale a alternativa que contém a análise correta.
Provas
O dióxido de nitrogênio (NO2) é uma molécula intermediária na produção industrial de ácido nítrico (HNO3), que é muito aplicado na produção de fertilizantes.
O dióxido de nitrogênio existe em equilíbrio com o tetróxido de nitrogênio (N2O4), segundo a reação:
!$ 2 NO_2(g) \rightleftarrows N_2 O_4(g)\,\,\,\,\,\triangle = -57,23 KJ/mol !$
Para aumentar o rendimento do dióxido de nitrogênio na reação, segundo o princípio de Le Châtelier, deve-se:
Provas
“Na última semana, os consumidores sentiram pesar no bolso o preço do gás de cozinha. O valor médio do botijão de 13 kg subiu de R$ 85,27 para R$ 85,63 entre os dias 6 e 12 de junho. Considerando todo o país, o maior preço do produto foi registrado na região Centro-Oeste, onde consumidores chegaram a pagar R$ 125 por um botijão.”
(Disponível em: https://jovempan.com.br/noticias/
brasil/ gas-de-cozinha-atinge-maior-preco-em-2021-e-deve-ficar-ainda-mais-caro-entenda-o-reajuste-da-petrobras.html. Acessado em 28/09/2021)
Supondo que todo o GLP presente no botijão seja somente butano e está totalmente na forma líquida, e que o preço do botijão de gás seja de R$ 125,00, para uma família que teve um gasto mensal com a fatura de gás de R$ 55,77, qual a quantidade de energia que foi liberada, em quilojoules, na queima do gás butano?
A reação de combustão completa do butano (não balanceada):
C4H10(g)→CO2(g)+H2O !$ \triangle H_C^{ \circ} = 2.808 KJ/ mol !$
Provas
A amônia ou amoníaco é um composto químico que na temperatura ambiente é um gás incolor, tóxico e corrosivo quando há presença de umidade. Esse gás, além de altamente perigoso no caso de inalado, também é inflamável. Muito utilizado na refrigeração e em processos de absorção em combinação com a água, além de seu uso na agricultura e em produtos de limpeza.
A amônia, ao reagir com a água origina os íons amônio e hidroxila, segundo o seguinte equilíbrio químico:
!$ NH_3(g) + H_2O( \ell) \rightleftarrows NH_4^+ (aq) + OH^- (aq) !$
Com relação à amônia e a sua reação com água, analise os seguintes itens:
I. A geometria molecular da amônia é piramidal.
II. A amônia é dita como base de Bronsted-Lowry na reação com a água.
III. NH4+ é a base conjugada da amônia.
Assinale a alternativa que contém a análise correta.
Provas
Niels Bohr (1885-1962) foi um físico dinamarquês, que estabeleceu o modelo atômico que em 1922 lhe valeu o Prêmio Nobel de Física. A partir dos estudos de Rutherford e da teoria da mecânica quântica da quantificação da energia proposto por Plank, Bohr estabeleceu o seu modelo atômico. A respeito dos postulados de Bohr, analise os seguintes itens:
I. Cada elétron apresenta uma quantidade específica de energia.
II. Um elétron absorve ou irradia energia conforme salta de uma órbita para outra. Se um elétron absorveu energia significa que ele saltou para uma órbita mais próxima do núcleo.
III. Para que o elétron permaneça em sua órbita a atração eletrostática entre o núcleo e o elétron deve ser igual a força centrífuga.
Assinale a alternativa que contém a análise correta.
Provas
A ureia ((NH2)2CO) é um composto orgânico, sólido, cristalino e solúvel em água. Ela tem diversas aplicações, como na alimentação de bovinos, estabilizador de explosivos, produção de resinas e medicamentos e até nas sínteses de fertilizantes agrícolas. Um dos meios de se obter a ureia e água é pela reação entre gás carbônico e amônia, nas condições adequadas.
Com base no texto, é correto afirmar que:
Provas
Caderno Container