Foram encontradas 760 questões.
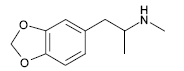
O ecstasy, cuja fórmula estrutural é mostrada acima, é uma droga psicoativa semi-sintética, da família das anfetaminas. Seu consumo provoca um grande efeito estimulante e pequenos efeitos visuais. É considerada principalmente uma droga de recreação, mas é usada também para práticas de transcendência — meditação, terapia psicodélica etc. O ecstasy é proibido em muitos países, incluindo o Brasil, e sua posse, produção ou venda pode resultar em processo criminal.
Considerando o texto acima e a fórmula estrutural do ecstasy, julgue os itens que se seguem.
O grupo ![]() , presente na molécula de ecstasy, é resistente ao ataque de nucleófilos e bases.
, presente na molécula de ecstasy, é resistente ao ataque de nucleófilos e bases.
Provas
Até meados do século XIX, as cirurgias eram realizadas sem anestesia, às vezes com a administração de quantidades apreciáveis de álcool, justificada pela crença de que o paciente ficaria entorpecido. Em 1846, William Morton conseguiu demonstrar que o éter dietílico podia ser usado para produzir inconsciência temporária durante os procedimentos cirúrgicos. Um problema dessa prática era o fato de o éter formar com o oxigênio do ar uma mistura explosiva, e qualquer choque entre os instrumentos metálicos cirúrgicos podia resultar em uma centelha e consequentemente em ignição. Outra substância usada como anestésico, o clorofórmio !$ H CC \ell_3 !$ 3 foi considerado melhor que o éter, pois a recuperação era mais rápida e menos desagradável. No entanto, alguns pacientes morriam; apesar disso, os riscos associados eram considerados pequenos. A partir de 1857, o clorofórmio tornou-se o anestésico preferido para os partos sem dor, na Europa e nos Estados Unidos. Atualmente, o clorofórmio não é mais usado para tal fim.
Acerca das substâncias citadas no texto, julgue o item a seguir.
O éter utilizado para produzir inconsciência temporária tem fórmula H3CH2COCH2CH3.
Provas
A sequência de equações parciais de I a V, a seguir, indicam a formação da salmoura — equação I e II —, a eletrólise da solução e a obtenção de hidróxido de sódio como subproduto.
I !$ Na C \ell(s) \overset{água} { \rightarrow} Na^+(aq) + C \ell^- (aq) !$
II !$ H_2 O ( \ell) \rightarrow H^+(aq) + OH^- (aq) !$
III reação anódica: !$ 2 C \ell^- (aq) - 2e^- \rightarrow 2[C \ell] \rightarrow C \ell_2(g) !$
IV reação catódica: !$ 2 H^+ (aq) + 2e^- \rightarrow 2[H] \rightarrow H_2(g) !$
V !$ Na^+(aq) + OH^- \overset{evaporação} {(aq) \rightarrow} Na OH(s) !$
Considerando as informações acima, julgue o item a seguir.
Se a eletrólise for conduzida com o sal !$ Na C \ell !$ fundido em substituição à solução de salmoura, os produtos da reação serão os mesmos da reação descrita no texto.
Provas
O processo de desenvolvimento de um fármaco inicia-se com a síntese e a determinação das características físico-químicas do princípio ativo. Essa análise inicial garante que a atividade observada nos ensaios in vivo é decorrente do princípio ativo no medicamento. A respeito dos parâmetros físico-químicos que podem ser utilizados durante o desenvolvimento de um xarope, julgue os itens a seguir.
A solução preparada é considerada uma mistura homogênea de espécies químicas dispersas em um solvente.
Provas
Em Baku, capital do Azerbaijão (ex-União Soviética) aconteceu uma das maiores tragédias já ocorridas em metrô: 337 pessoas foram mortas em conseqüência de um incêndio em 28/10/1995. O fogo atingiu os vagões lotados quando o tremestava entre duas estações, o que dificultou a fuga das vítimas. A maioria dos mortos foi envenenada pelo monóxido de carbono que infestou o ar do túnel.
Internet: <www.super.abril.com.br/revista/237> (com adaptações).
O monóxido de carbono (CO) é um gás incolor, sem cheiro e muito tóxico. Não é muito reativo, em grande parte, devido à sua entalpia de ligação (1.074 kJ × mol-1). O CO é muito usado na formação de complexos com átomos do bloco d da tabela periódica, pois ele pode formar ligações com esses átomos, tanto partilhando o par de elétrons isolados do carbono para formar uma ligação quanto utilizando seu orbital !$ \pi !$ antiligante para acomodar elétrons cedidos por esses átomos para formar uma ligação. Um complexo de CO muito conhecido é o níquel tetracarbonila (Ni(CO)4), um líquido formado em uma das etapas de um antigo processo de refino do níquel.
Segundo a teoria do campo cristalino, o complexo formado apresenta a configuração !$ e_g^4\,t_{2g}^4 !$ , ou seja, os dois orbitais eg têm energia abaixo da energia média enquanto os três orbitais t2g têm energia acima da energia média.
A formação de complexos é também responsável pela toxicidade do CO, que se liga mais fortemente ao ferro (II) do grupo heme na hemoglobina que o oxigênio e impede que o oxigênio do ar presente nos pulmões passe para a corrente sanguínea.
Considerando os textos acima, julgue o item seguinte.
A entalpia de ligação do monóxido de carbono é a variação de entalpia relacionada à reação representada pela seguinte equação química:
!$ C(grafite) +\,^1/_2 O_2(g) \rightharpoonup CO(g) !$
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
O processo de desenvolvimento de um fármaco inicia-se com a síntese e a determinação das características físico-químicas do princípio ativo. Essa análise inicial garante que a atividade observada nos ensaios in vivo é decorrente do princípio ativo no medicamento. A respeito dos parâmetros físico-químicos que podem ser utilizados durante o desenvolvimento de um xarope, julgue os itens a seguir.
Se duas preparações de xarope com concentrações diferentes do princípio ativo forem colocadas em contato por meio de uma membrana condutora, atingirão o equilíbrio térmico quando atingirem a mesma concentração do princípio ativo.
Provas
A sequência de equações parciais de I a V, a seguir, indicam a formação da salmoura — equação I e II —, a eletrólise da solução e a obtenção de hidróxido de sódio como subproduto.
I !$ Na C \ell(s) \overset{água} { \rightarrow} Na^+(aq) + C \ell^- (aq) !$
II !$ H_2 O ( \ell) \rightarrow H^+(aq) + OH^- (aq) !$
III reação anódica: !$ 2 C \ell^- (aq) - 2e^- \rightarrow 2[C \ell] \rightarrow C \ell_2(g) !$
IV reação catódica: !$ 2 H^+ (aq) + 2e^- \rightarrow 2[H] \rightarrow H_2(g) !$
V !$ Na^+(aq) + OH^- \overset{evaporação} {(aq) \rightarrow} Na OH(s) !$
Considerando as informações acima, julgue o item a seguir.
Nas espécies de hidrogênio — H+, [H] e H2 — da reação catódica, os átomos de hidrogênio apresentam diferentes números de prótons.
Provas
Durante a síntese de fármacos, a química orgânica é uma ferramenta muito importante porque permite a obtenção de moléculas em seus diversos níveis de complexidade. Entre as moléculas que tiveram uma grande importância na saúde pública destaca-se o sulfometoxazol, cuja estrutura é apresentada a seguir.
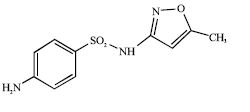
Considerando essas informações, julgue os próximos itens.
A fórmula geral do sulfometoxazol é C 10 H 11 N 3 O 3 S e a sua nomenclatura oficial IUPAC é 4 amino-N-(5-metil-3- isoxazolil-benzeno-sulfonamida).
Provas
A reação de Fenton ocorre no interior das células dos mamíferos segundo o mecanismo apresentado a seguir.
!$ Fe^{2+} + O_2 \rightleftharpoons Fe^{3+} + O_2^-\\2\,O_2^- + 2H^+ \rightarrow O_2 + H_2 O_2\\Fe^{2+} + H_2 O_2 \rightarrow Fe^{3+} + OH^- +OH^{ \cdot} !$
A respeito dessa reação, julgue o item seguinte.
A molécula OH- é denominada radical livre, porque possui elétrons desemparelhados.
Provas
A reação de Fenton ocorre no interior das células dos mamíferos segundo o mecanismo apresentado a seguir.
!$ Fe^{2+} + O_2 \rightleftharpoons Fe^{3+} + O_2^-\\2\,O_2^- + 2H^+ \rightarrow O_2 + H_2 O_2\\Fe^{2+} + H_2 O_2 \rightarrow Fe^{3+} + OH^- +OH^{ \cdot} !$
A respeito dessa reação, julgue o item seguinte.
A molécula OH- formada no meio aquoso apresenta características ácidas.
Provas
Caderno Container