Foram encontradas 1.397 questões.
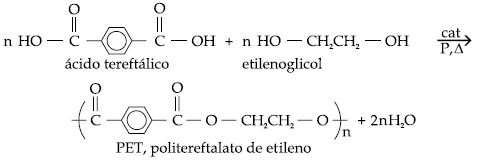
O politereftalato de etileno, PET, é um polímero de condensação resistente à corrosão por ácidos e bases, sendo utilizado como embalagem de água e de refrigerantes.
Provas
O petróleo é uma fonte renovável de hidrocarbonetos, e o craqueamento catalítico de moléculas desses compostos é realizado sob resfriamento constante e uso de catalisadores com propriedades ácidas.
Provas
A conversão de energia química em elétrica, com o uso de pilhas que utilizam eletrodos de mercúrio, cádmio ou zinco, é um processo sustentável de obtenção de energia, porque o consumo desses materiais diminui a extração de matéria-prima e não provoca impactos ambientais, quando descartados no ambiente.
Provas
| Equação da semirreação | Potencial padrão de redução, Eº (V) |
| Au3+(aq) + 3e- !$ \leftrightarrows !$ Au(s) | +1,42 |
| MnO4(aq) + 8H+(aq) + 5e- !$ \leftrightarrows !$ Mn2+(aq) + 4H2O(!$ \ell !$) | +1,49 |
De acordo com os potenciais padrão de redução apresentados na tabela, a reação entre o ouro e o íon permanganato, em meio ácido, é espontânea, e o !$ \Delta !$Eº desse processo é igual a +0,07V.
Provas
I. HNO2(aq) !$ \leftrightarrows !$ H+(aq) + NO-2 (aq) Ka = 5,0.10-4
II. H2CO3(aq) !$ \leftrightarrows !$ H+(aq) + HCO-3 (aq) Ka = 4,3.10-7
As constantes de equilíbrio dos sistemas químicos representados em I e II indicam que, em soluções aquosas 1,0mol.!$ \ell !$-1 dos ácidos nitroso e carbônico, a concentração de cátions e de ânions é maior no sistema I que no sistema II.
Provas
Fe2O3(s) + 3CO(g) !$ \leftrightarrows !$ 2Fe(s) + 3CO2(g)
Nas indústrias siderúrgicas, o ferro metálico é obtido nos altos-fornos, em determinadas condições, de acordo com o equilíbrio heterogêneo representado pela equação química, cuja constante de equilíbrio, Kc, é determinada pela expressão matemática
!$ Kc \, = \, \dfrac { [Fe]^2. \, [CO_2]^3} { [Fe_2O_3].[CO]^3} !$
Provas
Cl2(g) + 2NaOH(aq) NaClO(aq) + NaCl(aq) + H2O(!$ \ell !$)
A reação de obtenção do hipoclorito de sódio, NaClO, representada pela equação química em destaque, é de oxirredução, e a solução aquosa desse sal é vendida, comercialmente, como água sanitária, material utilizado no tratamento de água e na limpeza de ambientes.
Provas
O benzeno, C6H6(l) é um hidrocarboneto aromático, utilizado como solvente em laboratório, e, por ser reconhecidamente carcinogênico para o ser humano, deve ser utilizado com cautela.
Provas
| Substância química | Fórmula molecular | Ponto de Ebulição, ºC, 1atm. |
| Pentano | C5H12 | 36 |
| Hexano | C6H14 | 69 |
| Heptano | C7H16 | 98 |
O crescimento no valor dos pontos de ebulição dos hidrocarbonetos, apresentados na tabela, é justificado pelo aumento da intensidade nas ligações de hidrogênio presentes nas interações intermoleculares existentes nesses compostos.
Provas
A decomposição total de 492,0g de clorato de potássio, KClO3(s), de acordo com a equação 2KClO3(s) !$ \rightarrow \\ \Delta !$ 2KCl(s) + 3O2(g) produz 73,8!$ \ell !$ de gás oxigênio, O2(g), medidos a 27ºC e 1atm.
Provas
Caderno Container