Foram encontradas 13.432 questões.
Sabões são sais de sódio ou potássio de ácidos graxos, obtidos pela reação de gorduras e óleos (triglicerídeos) com \( NaOH \), \( KOH \) ou \( Na_2CO_3 \). A reação de saponificação é representada a seguir:
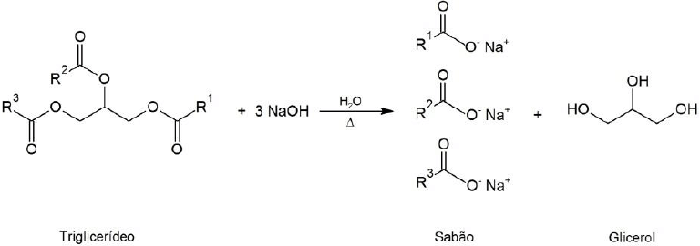
em que \( R^1 \), \( R^2 \) e \( R^3 \) são cadeias lineares saturadas ou insaturadas, geralmente com doze ou mais átomos de carbono.
Com base nessas informações, considere as seguintes afirmativas:
1. Uma solução aquosa de sabão puro apresenta pH < 7.
2. Adição de ácido forte a uma solução de sabão acarreta precipitação de ácidos graxos.
3. \( Ca(OH)_2 \) não pode ser usado na obtenção de sabão, pois sais de cálcio de ácidos graxos são insolúveis em água.
4. A obtenção de sabão com\( Na_2CO_3 \) segue a mesma estequiometria que no uso do \( NaOH \).
Assinale a alternativa correta.
Provas
A calda bordalesa, muito utilizada como fungicida na agricultura, é preparada pela mistura de sulfato de cobre pentaidratado \( (CuSO_4.5H_2O) \), um pequeno excesso de cal (CaO) e água em proporção de 1:1:10 (m:m:v), respectivamente, obtendo-se uma suspensão muito fina (partículas pequenas).
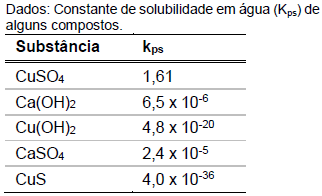
De acordo com os dados de constante de solubilidade, assinale a alternativa que apresenta o constituinte principal do sólido suspenso na calda bordalesa.
Provas
A utilização de conversores catalíticos no escapamento de automóveis diminui a emissão de gases tóxicos que são também geradores de compostos ácidos, como indicado nas seguintes equações:
\( 2CO + 2NO → 2CO_2 + N_2 \)
\( 2CO + O_2 → 2CO_2 \)
\( 2NO → N_2 + O_2 \)
Em um teste de laboratório, foram colocadas em um reator inextensível quantidades estequiométricas de \( CO \), \( NO \), \( O_2 \) e catalisador. Considerando que o experimento foi realizado nas CNTP, que os reagentes e os produtos são gases ideais e que a conversão foi de 100%, qual será a pressão final do sistema, em atm?
Provas
O ácido fosfórico \( (H_3PO_4) \) de alta pureza é obtido por via seca ou térmica, pela combustão do fósforo elementar e posterior hidratação do \( P_2O_5 \), de acordo com as reações abaixo:
\( 4P + 5O_2 → 2P_2O_5 \) \( ΔH= -720 \,kcal \)
\( P_2O_5 + 3H_2O → 2H3PO_4 \) \( ΔH= -45 \,kcal \)
Nesse processo, de acordo com as equações acima, assinale a alternativa que apresenta a quantidade de calor liberado na formação do \( H_3PO_4 \) (em kcal/mol).
Provas
A queima de enxofre elementar gera compostos gasosos responsáveis pela formação da chuva ácida, com consequente deterioração de edificações e de monumentos construídos em mármore, acompanhada de liberação de gás carbônico na atmosfera. Esse processo pode ser ilustrado pelas seguintes reações não balanceadas:
\( S + O_2 → SO_2 \)
\( SO_2 + O_2 → SO_3 \)
\( SO_3 + H_2O → H_2SO_4 \)
\( H_2SO_4 + CaCO_3 → CaSO_4 + H_2CO_3 \)
\( H_2CO_3 → CO_2 + H_2O \)
Considerando essa sequência de eventos, assinale a alternativa que apresenta a equação global balanceada dos eventos supracitados.
Provas
Alcanos podem ser obtidos em laboratório, pela reação de haletos de alquila em presença de sódio metálico (síntese de Wurtz), como indicado no esquema reacional abaixo:
2R-X + Na → R-R + NaX
Com base nesse esquema, assinale a alternativa que apresenta os possíveis produtos orgânicos da reação do 2-cloro-butano com o 3-cloro-pentano nas condições da síntese de Wurtz.
Provas
O índice de acidez (\( I_a \)) de óleos e gorduras é um dos parâmetros para a determinação de sua qualidade, visto que, quanto maior o grau de decomposição dos lipídeos, mais alta é sua acidez. Na determinação do Ia, uma quantidade conhecida de amostra \( (m_A) \) é dissolvida num solvente apropriado (p.e. etanol) e titulada com uma solução padronizada de NaOH de concentração \( C_B \), utilizando-se fenolftaleína como indicador. Sabendo que o \( I_a \) é definido como a massa de KOH (em miligramas) necessária para neutralizar 1 grama de amostra, dado pela equação
\( I_a = m_{KOH}(mg) / m_A(g) \),
e que o volume de solução de NaOH utilizado na titulação é \( V_B \), assinale a alternativa que apresenta a expressão para o cálculo do \( I_a \), de acordo com os dados obtidos experimentalmente.
Dados: massa molar do KOH = 56,1 g/mol
Provas
Artefatos de aço inoxidável são resistentes à corrosão devido a um fenômeno conhecido como passivação, que é a formação de uma fina camada de óxido de cromo na superfície, por ação do ar ou de oxidantes químicos. Sabendo-se que o ácido nítrico \( (HNO_3) \) na concentração de 1,6 mol/L pode ser usado como agente passivante, qual volume de \( HNO_3 \) concentrado (em litros) deve ser utilizado para a obtenção de 100 L de solução passivante?
(Dados: MM\( (HNO_3) \) = 63,0 g/mol; \( HNO_3 \) concentrado: d = 1,40 g/mL; teor máximo = 65%(m/m))
Provas
As atividades realizadas nos laboratórios didáticos de Química precisam ser acompanhadas do descarte correto dos resíduos produzidos durante as aulas experimentais, sendo importante classificar os resíduos e escolher o tratamento mais adequado. Nesse sentido, numere a coluna da direita de acordo com sua correspondência com a coluna da esquerda.
1. Resíduos básicos concentrados, p. ex. aminas.
2. Resíduos fortemente oxidantes em solução, p. ex. permanganato.
3. Resíduo de mercúrio metálico.
4. Resíduo contendo sais de cianeto em solução aquosa diluída.
( ) Tratar com sulfito de sódio e depois ajustar o pH entre 7 e 9.
( ) Recobrir o resíduo com enxofre em pó e armazenar.
( ) Diluir até obtenção de uma solução com pelo menos 50% de água (em volume) e, em seguida, ajustar o pH entre 7 e 9.
( ) Adicionar 1 grama de NaOH por 100 mL de solução. Adicionar água sanitária.
Assinale a alternativa que apresenta a numeração correta da coluna da direita, de cima para baixo.
Provas
O ácido nítrico “branco” (100% puro; P.E. = 83 ºC) pode ser obtido em laboratório por destilação de uma mistura de \( KNO_3 \) e \( H_2SO_4 \), como mostra a reação a seguir:
\( KNO_3 + H_2SO_4 → HNO_3 + KHSO_4 \)
Tendo em vista que o \( HNO_3 \) é decomposto por aquecimento a \( NO_2 \) e \( H_2O \), assinale a alternativa que apresenta a técnica de destilação que deve ser utilizada nesse processo.
Provas
Caderno Container