Foram encontradas 970 questões.
De acordo o Método de Análise e Solução de Problemas (MASP), relacione adequadamente as fases com seus procedimentos.
1. Identificar.
2. Observar.
3. Analisar.
4. Planejar.
5. Agir.
6. Verificar.
7. Padronizar.
8. Concluir.
( ) Treinar.
( ) Elaborar um Procedimento Operacional Padrão.
( ) Avaliar o resultado da ação proposta.
( ) Observar o problema.
( ) Refletir sobre todas as etapas.
( ) Investigar as causas do problema.
( ) Definir estratégias.
( ) Analisar as causas mais prováveis do problema.
A sequência está correta em
Provas
São características de imunoglobulinas específicas: se apresentam nas formas farmacêuticas solução ou pó liofilizado, estéreis e apirogênicos, com alta concentração de anticorpos específicos, derivados do plasma humano provenientes de indivíduos previamente imunizados ou hiperimunizados. O envase e a liofilização dos produtos hemoderivados sólidos devem ocorrer em quais ambientes?
Provas
“Em 30 de novembro de 2020, a Agência Nacional de Vigilância Sanitária (Anvisa) foi formalmente comunicada acerca da sua integração ao esquema de cooperação internacional em inspeções farmacêuticas, denominado Pharmaceutical Inspection Cooperation Scheme (PIC/S), a partir de 1º de janeiro de 2021. A Anvisa é a 54ª autoridade regulatória que integra o PIC/S, o que a torna protagonista na participação da elaboração de referências regulatórias de impacto internacional, aumentando o reconhecimento e a relevância das contribuições do Brasil no cenário mundial das Boas Práticas de Fabricação (BPFs) de medicamentos e insumos farmacêuticos. Segundo a Gerência Geral de Medicamentos e Produtos Biológicos (GGMED) da Anvisa, “a adesão do Brasil ao PIC/S contribuirá para a melhoria da qualidade e da imagem dos medicamentos produzidos no país, além de possibilitar o aumento da competitividade das empresas nacionais e seus produtos nos mercados internacionais.”
(Disponível em: <https://www.gov.br/anvisa/pt-br/assuntos/noticias-anvisa/2020/anvisa-e-aprovada-para-cooperacao-em-inspecao-farmaceutica-2013-pic-s>. Acesso em: 06/11/2021. Adaptado.)
São considerados objetivos da padronização de procedimentos e exigências regulatórias no contexto do PIC/S, EXCETO:
Provas
“A criação da Hemobrás se constituiu em estratégia governamental para o estabelecimento de centro de produção de hemoderivados no país. O plasma excedente do uso hemoterápico no Brasil, produzido pelos serviços que compõem a Rede Nacional de Serviço de Hemoterapia no âmbito do Sistema Nacional de Sangue (SINASAN), será destinado à Hemobrás, para fins do uso industrial.”
(Portaria nº 1.710/2020; Ministério da Saúde.)
Sobre a aquisição e distribuição de insumos para a produção de hemoderivados e para o seu registro e produção, analise as afirmativas a seguir.
I. As técnicas de DNA recombinante podem ser utilizadas no desenvolvimento de fatores da coagulação humana em substituição à sua obtenção por fracionamento do plasma humano.
II. Outros centros de produção de hemoderivados podem adquirir plasma diretamente do Sistema Nacional de Hemoterapia, desde que excedente à capacidade da produção da Hemobrás e mediante pagamento.
III. Em caso de ausência de tecnologia para fracionamento do plasma, é permitido contratar serviço nacional ou internacional para a sua realização.
IV. A produção de hemoderivados pode ser realizada a partir do plasma recuperado, pois ele mantém a integridade de proteínas e fatores de interesse.
V. A declaração da origem do plasma utilizado e o certificado da liberação da sorologia do plasma para fabricação dos hemoderivados são os únicos documentos que devem ser apresentados pela Hemobrás para fins de fiscalização pelo órgão sanitário.
Está correto o que se afirma apenas em
Provas
As informações contextualizam as questões 26 e 27. Leia-as atentamente.
“De acordo com o Documento de Trabalho QAS/20.842, de maio de 2020, da Organização Mundial de Saúde (OMS), ao contrário de outros insumos farmacêuticos, a água para uso farmacêutico é retirada de um sistema de purificação sob demanda e não está sujeita a ensaios de controle de qualidade para liberação antes do uso. Portanto, assegurar, manter e controlar a qualidade da água purificada conforme especificações farmacopeicas, a fim de atender a expectativa de produção on-demand, é mandatório. Para a Farmacopeia Brasileira, há três tipos de água para uso farmacêutico: a água purificada (AP); a água para injetáveis (API); e, a água ultrapurificada (AUP). O layout de um sistema de purificação de água na imagem possui três posições indicadas: I, II e II.”
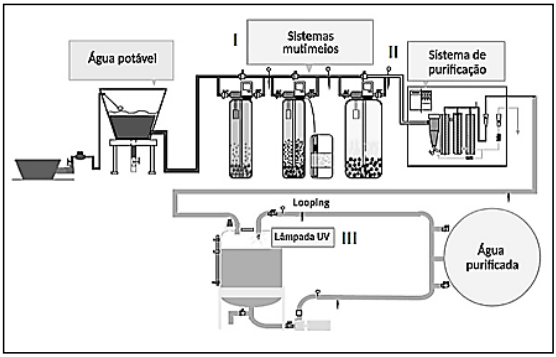
(Layout representativo de um sistema de purificação de água. Disponível em: <https://microambiental.com.br>. Acesso em: 04/11/2021. Adaptado.)
Assinale a afirmativa correta.
Provas
As informações contextualizam as questões 26 e 27. Leia-as atentamente.
“De acordo com o Documento de Trabalho QAS/20.842, de maio de 2020, da Organização Mundial de Saúde (OMS), ao contrário de outros insumos farmacêuticos, a água para uso farmacêutico é retirada de um sistema de purificação sob demanda e não está sujeita a ensaios de controle de qualidade para liberação antes do uso. Portanto, assegurar, manter e controlar a qualidade da água purificada conforme especificações farmacopeicas, a fim de atender a expectativa de produção on-demand, é mandatório. Para a Farmacopeia Brasileira, há três tipos de água para uso farmacêutico: a água purificada (AP); a água para injetáveis (API); e, a água ultrapurificada (AUP). O layout de um sistema de purificação de água na imagem possui três posições indicadas: I, II e II.”

(Layout representativo de um sistema de purificação de água. Disponível em: <https://microambiental.com.br>. Acesso em: 04/11/2021. Adaptado.)
Para reduzir os riscos associados à qualidade da AP em relação à sua produção, armazenamento e distribuição, é correto afirmar que é essencial:
Provas
Em relação às Parcerias para o Desenvolvimento Produtivo (PDP), analise as afirmativas a seguir.
I. O registro do medicamento ou produto para a saúde na Agência Nacional de Vigilância Sanitária (Anvisa) deverá constar no cronograma das PDP para transferência de tecnologia.
II. Compete ao Presidente da República definir os bens e produtos estratégicos para o SUS, que serão objeto das PDP, mediante publicação de listas propositivas de produtos a serem priorizados nas parcerias.
III. Seu prazo de vigência não excederá dez anos, salvo nos casos em que o prazo do desenvolvimento tecnológico seja reconhecidamente superior ao limite estabelecido e que a PDP resulte na nacionalização de um produto de alta importância para o país.
Está correto o que se afirma apenas em
Provas
De acordo com a Lei nº 14.303/2020, as contratações públicas deverão submeter-se a práticas contínuas e permanentes de gestão de riscos e de controle preventivo. Diante do exposto, assinale a afirmativa INCORRETA.
Provas
O Registro de Preços Nacional (RPN) constitui em instrumento administrativo que abrange a elaboração de especificações, estudo de mercado, realização da licitação e gestão de atas de registro de preços a serem disponibilizadas aos órgãos participantes de compra nacional. Assinale a afirmativa INCORRETA, considerando o Decreto nº 7.892/2013.
Provas
De acordo com a Lei nº 10.520/2002, para a aquisição de bens e serviços comuns, poderá ser adotada a licitação na modalidade Pregão. Em relação a tal modalidade, assinale a afirmativa correta.
Provas
Caderno Container