Foram encontradas 2.308 questões.
Observe o ponto de ebulição e a basicidade dos compostos nitrogenados mostrados a seguir.
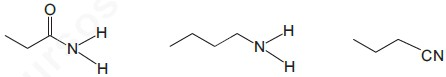
A esse respeito, é correto afirmar que a
Provas
Um processo de alquilação utilizado nas refinarias de petróleo para a produção de gasolinas com alta octanagem consiste da reação de isobutano com isobuteno, catalisada por ácido sulfúrico.
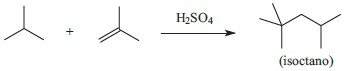
Sobre as principais etapas envolvidas nesse processo de alquilação, o ácido sulfúrico protona uma molécula de
Provas
Sabendo que a dissolução de 0,3 g de uréia em 10,0 g de água provoca uma alteração de aproximadamente 0,3 ºC no ponto de ebulição da água, considere as afirmações a seguir.
I - Uma solução 0,5 molal de uréia em água terá ponto de ebulição normal de aproximadamente 100,3 ºC.
II - Uma solução 0,5 molal de NaCl em água terá ponto de ebulição normal de aproximadamente 100,3 ºC.
III - A solubilização de 0,3 g de KCl em 10 g de água acarretará uma elevação na temperatura de ebulição da água de, aproximadamente, 0,3 ºC.
IV- A solubilização de 0,6 g de uréia em 10 g de água acarretará uma elevação na temperatura de ebulição da água igual a 0,6 ºC.
(Dados: Ponto de ebulição normal da água: 100 ºC; Ke = 0,5 ºCm-1; !$ \Delta !$Te = Ke.m; Massa molecular da uréia = 60 gmol-1)
Estão corretas APENAS as afirmações
Provas
O zinco é um metal amplamente utilizado na galvanização, principalmente, de ferro e aço. Nesse processo de eletrodeposição, o material a ser protegido deve ser colocado
Provas
As propriedades coloidais são, geralmente, exibidas por dispersões de substâncias com tamanhos de partícula entre 0,1!$ \mu !$m e 1nm. Considere as afirmações a seguir, relativas às propriedades características da maioria das partículas coloidais.
I - Não podem ser separadas das soluções pelo processo de diálise.
II - Podem provocar o espalhamento de luz incidente.
III - São retidas em papel de filtro comum.
IV- Possuem cargas elétricas e podem migrar sob a influência de potencial adequado.
Estão corretas APENAS as afirmações
Provas
Analise as afirmações a seguir.
É possível distinguir a força ácida de HBr e HI em água.
PORQUE
HBr e HI transferem de forma praticamente completa os seus prótons para a água, formando H3O+.
A esse respeito conclui-se que
Provas
A distribuição da energia cinética molecular em duas temperaturas distintas pode ser vista na figura a seguir.
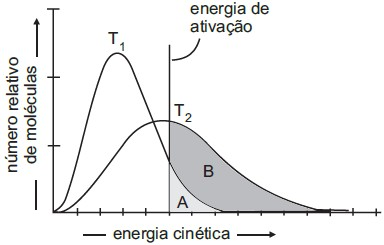
Sabendo que a temperatura de um sistema é a medida da energia cinética média de todos os átomos e moléculas presentes no sistema, considere as seguintes afirmações a respeito das temperaturas T1 e T2 mostradas no gráfico:
I - T1 >T2 porque, em qualquer sistema, somente um pequeno número de moléculas pode apresentar energia cinética maior do que a energia de ativação, como exemplificado na região A.
II - T2>T1 porque a região B apresenta um maior número de moléculas com energia cinética maior do que a energia de ativação.
III - T1>T2 porque a área total sob a curva na temperatura T1 é maior do que a área sob a curva na temperatura T2.
Está(ão) correta(s) APENAS a(s) afirmação(ões)
Provas
Sabendo que a entalpia de rede dos sais é inversamente proporcional à distância entre os centros dos íons
!$ \Delta !$Hr !$ \approx !$ 1/(R+ + R–)
e que a diferença de tamanho dos íons favorece a solubilidade do sal em água, é correto afirmar que
| Solubilidade em água |
Provas
A razão de compressibilidade, Z, de um gás é a razão entre o volume molar do gás e o volume molar de um gás ideal nas mesmas condições de temperatura e pressão. A figura a seguir mostra a variação no fator de compressibilidade de alguns gases em função de variações na pressão.
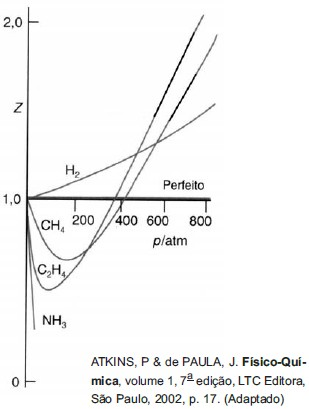
Com base nas informações contidas no gráfico, analise as afirmações a seguir.
I - Na pressão de 200 atm, as forças repulsivas são predominantes nas moléculas de H2.
II - Nos níveis de pressão indicados, as moléculas de amônia sempre apresentam predominância de forças atrativas.
III - Um gás ideal deveria apresentar Z = 0, pois não há qualquer tipo de interação entre suas moléculas.
Está(ão) correta(s) APENAS a(s) afirmação(ões)
Provas
Em temperaturas elevadas, a azida de sódio decompõe-se vigorosamente a sódio metálico e nitrogênio gasoso. Este comportamento é aproveitado nos dispositivos do tipo airbag, presente em alguns automóveis. Quando ocorre um impacto, uma corrente elétrica é disparada e provoca o aquecimento da azida que se encontra no interior do dispositivo, que é então inflado pelo nitrogênio liberado na reação de decomposição mostrada a seguir.
2 NaN3 !$ \xrightarrow {\text{aquecimento}} !$ 2 Na + 3 N2
Considerando um airbag que contenha aproximadamente 65 g de NaN3, o volume de nitrogênio (em litros), produzido quando a azida é detonada na temperatura e pressão ambientes (20 ºC e 1 atm) é, aproximadamente, igual a
(Dados: PV = nRT. Considerar que o nitrogênio se comporta como um gás ideal).
Provas
Caderno Container